La sinusite œdémato-purulente : y penser !
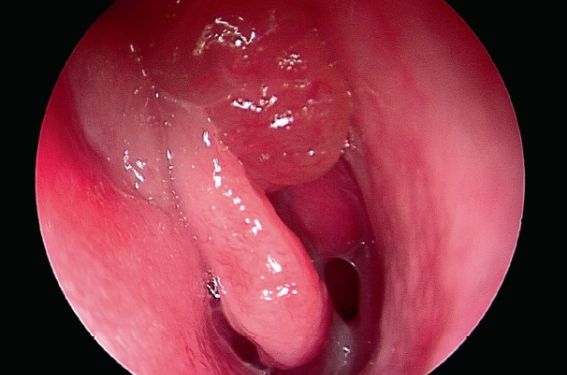
Avec une prévalence globale estimée à 10,9 %, les rhino-sinusites chroniques (RSC) constituent un des motifs de consultation les plus fréquents en ORL. Une RSC est définie par la présence, pendant plus de 12 semaines consécutives, de deux ou plus des symptômes suivants : obstruction ou congestion nasale, rhinorrhée antérieure ou postérieure, céphalées ou pesanteur faciale, troubles quantitatifs de l’odorat, toux(1). Lorsqu’un patient porteur d’une polypose naso-sinusienne présente des surinfections répétées ou lorsque le traitement antibiotique s’avère inefficace une sinusite œdémato-purulente doit être évoquée et une pathologie sous-jacente recherchée.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante



